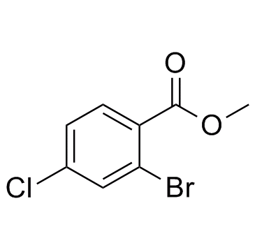
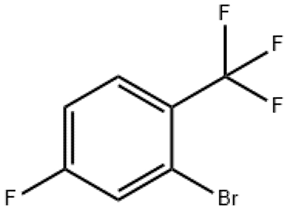
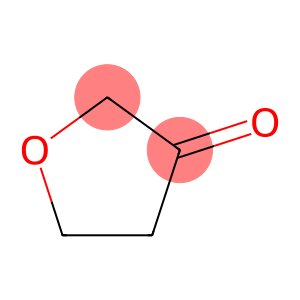
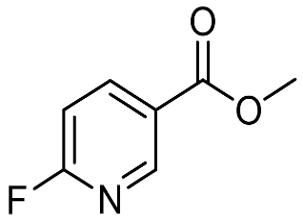
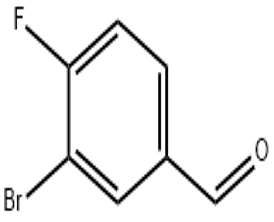
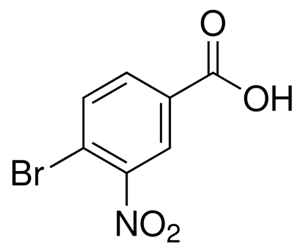
alfa-ionon(CAS#127-41-3)
| Risk kodları | R42/43 – Tənəffüs və dəri ilə təmasda həssaslığa səbəb ola bilər. |
| Təhlükəsizlik Təsviri | S24/25 – Dəri və gözlərlə təmasdan çəkinin. |
| WGK Almaniya | 2 |
| RTECS | EN0525000 |
| TSCA | Bəli |
| HS kodu | 29142300 |
alfa-ionon(CAS#127-41-3) məlumat
Benzofenon kimi də tanınan bənövşəyi keton üzvi birləşmədir. Budur ionon haqqında bəzi təhlükəsizlik məlumatları:
1. Toksiklik: Bənövşəyi keton insan orqanizmi üçün müəyyən toksikliyə malikdir. Mərkəzi sinir sisteminə və qaraciyərə zərər verə bilər, reproduktiv sistemə və embrionlara mənfi təsir göstərə bilər.
2. İnhalyasiya təhlükəsi: İononun buxarını və ya tozunu tənəffüs etmək başgicəllənmə, yuxululuq, öskürək və nəfəs almaqda çətinlik kimi xoşagəlməz simptomlara səbəb ola bilər. Uzun müddət məruz qalma mərkəzi sinir sisteminə zərər verə bilər.
3. Təmas təhlükəsi: Bənövşəyi keton dəri vasitəsilə sorula bilər. Uzunmüddətli və ya geniş təmas dərinin və gözün qıcıqlanmasına səbəb ola bilər. İononla işləyərkən əlcəklər və qoruyucu eynəklər kimi müvafiq fərdi qoruyucu vasitələrdən istifadə edilməlidir.
4. Yanğınsöndürmə tədbirləri: Sızma və ya yanğın zamanı yanğını söndürmək üçün quru toz, köpük və ya karbon qazından istifadə edin. Sudan istifadə etməyin, çünki bənövşəyi keton su ilə reaksiyaya girərək yanan qazlar əmələ gətirir.
5. Tullantıların utilizasiyası: Bənövşəyi keton tullantılarını yerli qaydalara və qaydalara uyğun olaraq düzgün şəkildə atın. Onu kanalizasiyaya və ya zibil qutusuna atmayın.
6. Saxlama tədbirləri: Bənövşəyi keton sərin, quru, yaxşı havalandırılan yerdə, yanğın mənbələrindən və oksidləşdiricilərdən uzaqda saxlanmalıdır.
Bu məlumatlar yalnız istinad üçündür. İononun əlavə istifadəsi və ya emalı tələb olunarsa, lütfən, müvafiq təhlükəsizlik məlumat vərəqinə müraciət edin və bir mütəxəssislə məsləhətləşin.
təbiət
Linaylketon kimi də tanınan bənövşəyi keton təbii keton birləşməsidir. Bənövşəyi çiçəklərin ətirinin əsas komponentidir.
Bənövşəyi keton otaq temperaturunda uçucu olan rəngsizdən açıq sarıya qədər yağlı mayedir.
Bənövşəyi keton spirtdə və efir həlledicilərində, suda az həll olunur. Onun sıxlığı nisbətən aşağıdır, sıxlığı 0,87 q/sm³-dir. İşığa həssasdır və ultrabənövşəyi şüaları uda bilir.
Bənövşəyi keton kimyəvi reaksiyalarda keton spirtlərinə və ya turşulara oksidləşə bilər və hidrogenləşmə reduksiya reaksiyaları vasitəsilə spirtlərə çevrilə bilər. Bir çox birləşmələrlə alkilləşmə və esterləşmə reaksiyalarına məruz qala bilər.
Tətbiq və sintez üsulu
Bənövşəyi keton (həmçinin bənövşəyi keton kimi tanınır) aromatik keton birləşməsidir. Xüsusi bir qoxuya malikdir və tez-tez ətir və ətir sənayesində istifadə olunur. Aşağıda iononun istifadəsi və sintez üsullarına giriş verilmişdir:
Məqsəd:
Ətir və ədviyyat: bənövşəyi ətirli məhsulların istehsalı üçün ətir və ədviyyat sənayesində geniş istifadə olunan iononun ətir xüsusiyyətləri.
Sintez üsulu:
İononun sintezi ümumiyyətlə aşağıdakı iki üsulla əldə edilir:
Nukleobenzolun oksidləşməsi: Nukleobenzol (metil əvəzedicisi olan benzol halqası) ionon yaratmaq üçün oksidləşdirici turşu və ya turş kalium permanqanat məhlulundan istifadə etməklə oksidləşmə reaksiyasına məruz qalır.
Pirilbenzaldehidin birləşməsi: Pirilbenzaldehid (para və ya meta vəziyyətdə olan piridin halqası əvəzediciləri ilə benzaldehid kimi) ionon yaratmaq üçün qələvi şəraitdə sirkə anhidrid və digər reaktivlərlə reaksiyaya girir.